【トピックス】
シームレスカプセル技術とその応用
田川大輔
森下仁丹株式会社
1.はじめに
森下仁丹 (株) は、1970年代から独自の同心二重ノズルを用いた滴下法による二層シームレスカプセル化技術の開発を始めた。1980年代に液体仁丹の実用化に目処が立ち、さらに、各種香料精油のカプセルを口中清涼剤、菓子やチューインガムへと展開して行った。また、食品素材による耐酸性カプセル皮膜開発にも着手した。同時にその技術を利用する有意性のある内容物を検討し、当時認知度は低かったが、ビフィズス菌のお腹における有用性と酸に弱いという菌の性質に着目した。ビフィズス菌を生きたまま腸まで届けることができると人々の健康に寄与できると考え、製剤研究開発を推進した。その研究により、同心三重ノズルを用いて外側の皮膜、内側の皮膜、さらに内容物という構造の三層カプセルを開発した。この技術は、従来の軟カプセルの製法とは異なり、同心多重ノズルの先端より充填物質と皮膜物質を同時に滴下させて、皮膜液のゾル−ゲル転位により液滴形成と硬化 (カプセル化) を同時に行う技術である。同心ノズルを二重から三重にすることで、シームレスカプセルの皮膜を二層にして三層カプセルとすることが可能になり、酸性の胃では溶けず腸で溶けるいわゆる腸溶性カプセルが開発された。この三層の腸溶性カプセルに酸に弱いビフィズス菌を包むことで、胃酸から保護し、高効率で生きたまま腸に運ぶことができるようになり、これまでにない整腸作用を示し、機能性食品や医薬品として用いられている。
近年は本技術を用いて非可食分野への展開にも成功している。
本稿では、森下仁丹シームレスカプセル化の技術を解説し、ユニークな応用例についても紹介する。
2.シームレスカプセルの製造方法
医薬品や食品で、一般的に広く用いられるカプセルには、「硬カプセル (ハードカプセル) 」や「軟カプセル (ソフトカプセル) 」がある。硬カプセルは、医薬品で多く利用されているもので、ボディとキャップを組み合わせる形式であり、主に粉末や顆粒をボディに封入し、キャップをはめ込むように製造される。一方、軟カプセルは、健康食品で多く利用されており、親油性の液体や油脂に懸濁した粉末などをロータリーダイにより打ち抜き製造される継目のあるラグビーボール型 (最近は多様な形のものがある) のカプセルである。いずれのカプセルも複数のパーツを組み合わせたあるいはつなぎ合わせた皮膜となっている点に特徴がある。
一方、シームレスカプセルは、継ぎ目のない真球状のカプセルであり、継ぎ目から外部の液体などが侵入することがないため、内容物を外部環境から保護する用途に適している。前述のカプセルとは製法が異なり、「液中滴下法」と呼ばれる方法で製造される。「液中滴下法」とは、界面張力を利用した製造方法である。この液中滴下方式では、ノズルを二重から三重にすることによりカプセル中心部の充填物質と最外層の皮膜との間に新たな物質層を介在させることが可能となり、三層構造のシームレスカプセルを量産することが容易である。図1 の (A) にカプセル製造機の模式図を、 (B) に三重ノズル部の断面拡大図を示す。流下するキャリアー液 (冷却液) に同心多重ノズルを挿入し、この多重ノズルの内ノズルから充填内容物質、外側ノズルから皮膜物質をそれぞれ流動状態で同時に吐出し、界面張力を利用し球形のカプセルを形成する。カプセルの粒径は0.5〜8 mmの範囲で自由に設定が可能である。また、皮膜の厚さも自由に設定でき、粒径3 mmでは皮膜を30μmまで薄くしたカプセルを調製している。
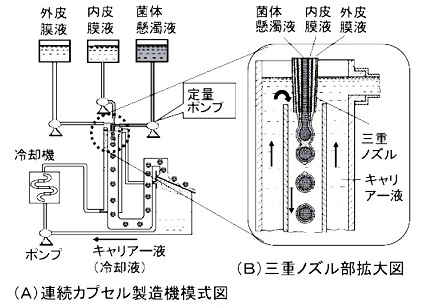
図1 シームレスカプセル製造フロー
皮膜物質としては、温度の違いにより溶液状態 (ゾル) から固化 (ゲル化) する物質が利用される。例えば食品の場合、ゼラチン、寒天等の水溶性高分子である。この皮膜物質を工夫することで、耐酸性、耐凍性、耐熱性などの対環境性能の向上や、温度やpH応答性などによる崩壊条件の制御を付与した、例えば腸溶性などの機能をもったシームレスカプセルを製造することが可能となる。近年はUVにて樹脂化する物質も利用可能となり、耐久性の必要となる分野にも適用できるようになった。
ノズルを多重にすることで、二層、三層、四層のカプセルを形成することが可能であり、各層は界面が形成される物質の組み合わせであればよいので、内容物としては、親油性物質、親水性物質のいずれも包み込むことができる。食品の場合、このような特長を組み合わせることで、内容物の特性、利用率、飲みやすさを考慮したキャリアーとすることができる。また、充填物質や皮膜の重量の均一性にも優れている。このように、シームレスカプセルの液中滴下法は従来のソフトカプセルの製法であるロータリー法に比べて製剤設計の自由度が高く、皮膜に特性を付与することもできる生産性に優れた製法であると言える。
3.シームレスカプセルの機能と特性
多層シームレスカプセルの調製において、層間の境界面を明確に形成することが重要であり、そのためにはエマルジョン形成と同様に二層であればO/W (Oil/Water)、三層であればW/O/W (Water/Oil/Water) またはO/W/Oのように界面張力が交互に作用する組み合わせにすればよい。例えば外皮膜には水溶性のポリマーを、内皮膜には油性の皮膜物質を用いれば水性の内容液のカプセルを形成できる。得られるカプセルの例を図2 に示したが、O/W/O/W にすることで、世界初の四層カプセル (カプセル in カプセル、図2の右端) の調製にも成功している。これは外側の皮膜が口で溶けて外の成分を放出し、内部のカプセルの皮膜は胃で溶けて内側の成分を放出するような、二成分を別々の場所で作用させる機能を持ったカプセルである。これら多層構造カプセルの機能発現要素には、皮膜層素材と層厚があり、これらの組み合わせにより充填成分の隔離保護あるいは放出の幅広いコントロールが可能である。特に耐酸性を持たせた親水性の外皮膜と油性の内皮膜を用いて胃酸の侵入をブロックするカプセルは、 お腹に重要なビフィズス菌を生きたまま腸に届ける用途のカプセルとして用いられている。また、新たな機能として注目されるのは、カプセル内で細胞を培養増殖させることができることであり、ビフィズス菌や植物細胞のカプセル内高密度培養に成功し、その応用展開を進めている。
その他、シームレスカプセルは、様々な機能を発現可能である。実際の使用例を基に発現可能な機能の一例を以下に紹介する。

図2 シームレスカプセルの例
3-1 遮蔽効果
カプセルを用いることで、通常は同一空間に共存できない複数の物質を共存させることが可能である。例えばある物質Aの中に、物質Bを内包したカプセルを分散させることで、物質Aに物質Bの特性を付与できる。例えば、蓄熱物質を内包させてカプセルを樹脂等に分散させることで、樹脂に蓄熱性能を付与することが可能となる。
3-2 リリースコントロール
カプセルは、ある物質を狙ったタイミングで放出することが可能である。放出するにはカプセルの皮膜を崩壊させる必要があり、薬剤等のドラックデリバリーシステムでは体内でのpHの変化等により皮膜を崩壊させることが多い。皮膜崩壊のトリガーとしては、pH以外にも圧力 (シェア)、熱等を使用できる。
3-3 物質吸収
カプセルの皮膜に透過性の物質を使用し、カプセルの中にターゲット物質と相互作用を発現する物質を内包させることで、吸着剤として使用することが可能である。シームレスカプセルは固体状、液体状等様々な性状の物質を内包させることが可能であり、通常は吸着剤として使用困難な物質を、吸着剤として使用可能となる。
3-4 マイクロリアクター
3-3と同様半透膜の皮膜を使用し、カプセル中に触媒等の反応促進剤を内包させることで、カプセル内で様々な反応を起こすことが可能である。パラジウム触媒内包カプセル内でのカップリング反応や、微生物を内包カプセル内で酵素反応を行うことに成功した。
4.生きた乾燥ビフィズス菌末のカプセル化
生きたビフィズス菌カプセルは、三重ノズルを用いた液中滴下法で調製される。外皮膜素材としては、水溶液が加熱により溶液状態になり、冷却することにより固化するゼラチンなどの水溶性高分子が用いられてきたが、現在はデンプンなどの植物性素材が用いられている。その内側のバリアー層となる内皮膜には融点の高い硬化油が用いられ、さらに、凍結乾燥ビフィズス菌末を融点の低い硬化油に懸濁したものが内容液となっている。加温して溶融状態にある内容液および内外の皮膜液は、それぞれのタンクから定量ポンプで同心三重ノズルに送られる。キャリアー液 (冷却液) は0〜10℃に冷却された液状油が用いられ矢印の方向に沿って循環している。図1 (B) の拡大図に示すように三重ノズルの内ノズルから内容液、中間ノズルから内皮膜液、最外層から外皮膜液が三相ジェットとして同時にキャリアー流体中に吐出される。吐出された三相ジェットは界面張力によりビフィズス菌を懸濁した内容液を内包した球となり,形成管中を流下していく過程で各液が冷却され固化する。固化したカプセルは分離器でキャリアー液と分離され、クーリング、脱油、 乾燥、選別の各工程を経て製品化される。得られる乾燥ビフィズス菌の三層カプセルの模式図を図3に示す。
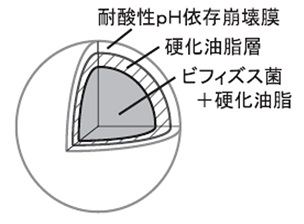
図3 ビフィズス菌カプセルの模式図
5.バイオカプセルの開発
この同心三重ノズルを用いた水系物質をカプセル化できる技術を発展させ、水中で安定な半透性を有するゲルを形成する外皮膜に用い、二層皮膜で生きた細菌の菌体培養懸濁液を包括することが可能になった。このような生きた細胞の菌体を包括した微小培養槽ともいうべきカプセルを「バイオカプセル」と称しているが、菌のカプセル内培養増殖は皮膜の半透性を利用した一種の透析培養である (図4)。すなわち、カプセルを栄養培地に浸けることで外の培地中から栄養素をカプセル内に供給することができ、老廃物は外部に拡散希釈されるため、カプセル内でビフィズス菌を高密度に増殖させ得る。
更にはカプセルをカラムに充填し、外部タンクから培地を循環させることによって培養するバイオリアクターシステムを構築した。
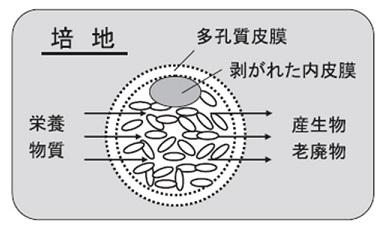
図4 バイオカプセルのカプセル内培養増殖模式図
6.シームレスカプセルの応用例
6-1 ビフィズス菌カプセル
ビフィズス菌は、腸内有用菌であり、プロバイオティクス (宿主の腸内細菌叢のバランスを改善する事により、宿主に有益な作用をもたらす生きた微生物) として、ヨーグルトやサプリメントに利用されているが、酸に弱いことが知られている。つまり、ビフィズス菌を経口で摂取した場合、pHの低い胃酸により生存率が低下し、作用部位である腸まで生きたまま届けることが困難であると考えられる。そこで、腸溶性シームレスカプセルのデリバリーシステムとしての利用による到達率の向上が期待される。ビフィズス菌を配合したシームレスカプセルは、三層で構成される。最外層には、酸性領域では溶解しないが中性領域で溶解する物質 (ペクチン等) を使用することでpH応答性により、胃で溶けず腸で溶けるよう設計している。中間層には硬化油脂を使用し、胃酸などの透過に対するバリアー機能の向上を図っている。最も内側の層に内容物 (ビフィズス菌乾燥菌末) を封入し、前述の最外層および中間層の二層によるデリバリーシステムを実現している。ビフィズス菌凍結乾燥菌末のような粉末を内容物にする場合は、油脂等に懸濁することで、液中滴下法により連続してシームレスカプセル内に封入し、製造することが可能となる。
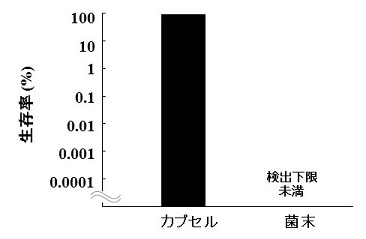
このように作製された腸溶性シームレスカプセル (直径約2 mm) では、人工胃液中でビフィズス菌の高い生存率を示す。日本薬局方溶出試験法に用いられる溶出試験装置を使用し、pH1.2の人工胃液 (日本薬局方溶出試験第1液を使用) 中に、ビフィズス菌の凍結乾燥菌末を包含したカプセルを加え、2時間撹拌を行った後の生存率を検証すると、90%という高い生存率を示すことが明らかとなっている。このとき、凍結乾燥菌末のみで検証すると、その生存率は0.00007%以下であり、腸溶性シームレスカプセルにより高い耐酸性を付与できることが示されている (図5)。腸溶性シームレスカプセルは、pHの低い胃を通過した後、腸に届くころ、pHが中性付近に変化することで、pH応答性を有する皮膜が溶解する。その後、中間層が、胆汁酸やリパーゼによる分解を受け、さらに腸管運動による物理的刺激も加わり崩壊し、ビフィズス菌が作用部位である腸まで届くものと考えている。

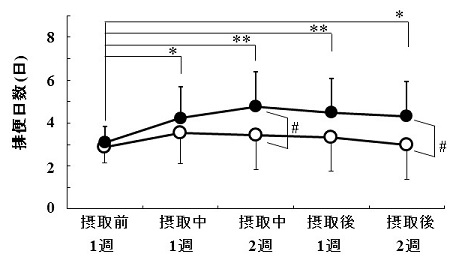
ビフィズス菌カプセルを摂取することで、実際にヒトでも排便回数の増加などの効果が認められている。非腸溶性の硬カプセルあるいは腸溶性シームレスカプセルに配合された同菌数のビフィズス菌を、大学生を対象として、2週間摂取させた試験では、腸溶性シームレスカプセル配合ビフィズス菌摂取により、1週間毎の排便回数が、摂取1週目から有意に増加し、摂取2週目 (p<0.05)、摂取中止後の2週間においても有意な増加を維持した。さらに、摂取2週目には、非腸溶性硬カプセルに配合されたビフィズス菌摂取群との比較においても、有意に多い排便日数を示した (p<0.05) ことが報告されている1) (図6)。

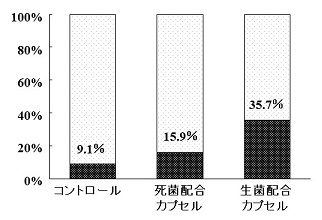
また、ビフィズス菌の生菌と死菌を摂取した際の比較検証も、健常成人10名 (平均年齢56.8歳) を対象として、行われている。腸溶性シームレスカプセル配合生菌を2週間摂取したところ、摂取前に比べ、糞便中総菌数に占めるビフィズス菌の割合 (占有率) が9.1%から35.7%へ増加するが、同菌数の死菌を配合した腸溶性シームレスカプセルを摂取した場合、摂取後のビフィズス菌占有率は15.9%であり、生菌配合の腸溶性シームレスカプセルの方が、効率的に腸内ビフィズス菌を増加させることが示されている2) (図7)。
これらはいずれも、腸溶性シームレスカプセルがデリバリーシステムとして効果を発揮し、ビフィズス菌を生きたまま腸まで届けることで、効率的な腸内環境、便通改善につながることを示す結果と考えられる。

6-2 レアメタル・貴金属回収カプセルの開発
大阪府立大学大学院の小西らが開発した、金属イオン還元細菌 (Shewanella algae) を金属遊離菌体として用いるレアメタル回収法においては、回収した金属を含有する細菌細胞 (短軸径 0.5μm×長軸径1.0μm程度) が微粒子であるうえに、細胞密度が水と同程度であるために細菌細胞の固液分離は容易でないことから、煩雑な分離操作 (ろ過、遠心分離など) が別途必要になる。この煩雑さを避ける方策として、前述の「バイオカプセル」技術を用い、還元細菌を内包するシームレスカプセル (図8) を産学連携で開発した。ターゲット金属を透過する皮膜で構成されるカプセルの内部溶液に還元細菌を包み込むことで、有用金属を分離・濃縮した細菌細胞の固液分離は「カプセルを網ですくう」程度の簡単な操作で完了する。この微生物カプセルの利用によって、リサイクル現場において還元細菌のハンドリングが簡便になる,また分離・回収プロセスがコンパクトになる等の大きなメリットが得られる。
還元細菌を内包するシームレスカプセル (図9) は、物理的に強固で、幅広いpH領域でも長期間安定であり、回収ターゲット金属イオンが溶液からカプセル内部に効率的に透過するように皮膜構造 (網目サイズ,膜厚み) を調整することも可能である。ただし、還元細菌が外部溶液に透過できないように、皮膜の網目サイズは細胞径 (0.5μm×1.0μm) 以下にする必要がある。
微生物カプセルによる貴金属・レアメタル回収速度は、遊離菌体の場合に比べると遅くなるが、従来法 (イオン交換樹脂による吸着分離) よりも速くなる。今後、カプセルの皮膜成分 (親疎水性) ならびに皮膜構造 (網目サイズ、膜厚み等) を最適化することにより、レアメタル回収速度をさらに高めることは十分に可能である。
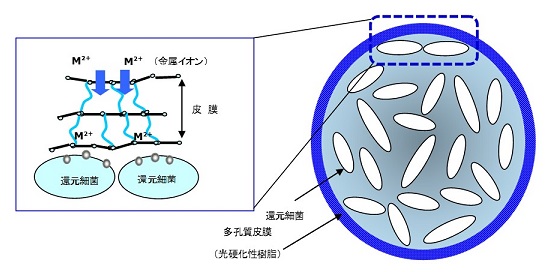
図8 金属イオン還元細菌を内包したシームレスカプセルの模式図
6-3 環境浄化カプセルの開発
環境浄化方法の一つとして、微生物の機能を利用して汚染物質を分解するバイオレメディエーションが知られている。バイオレメディエーションには、大別して、土着の微生物を活性化させて利用する方法 (バイオスティミュレーション) と、汚染物質を分解する微生物を外部から投入する方法 (バイオオーグメンテーション) とがあるが、前者は浄化能力が弱く、後者は外来微生物をばらまくことへの懸念や、土着微生物との競合により外来微生物が十分に生存できないなどの問題がある。
バイオレメディエーションの方法としては、ポリビニルアルコールなどのゲル材料やウレタンフォーム、活性炭などの担体に目的の微生物を表面固定法や包括法によって固定化して得られる微生物固定化担体を用いる方法や、目的の微生物を充填した水溶性の合成樹脂製カプセルを用いる方法などが開発されている。しかしながら、表面固定法によって固定化された微生物は、環境に投入後に担体から固定化微生物が遊離することがあり、包括法によって固定化された微生物やカプセルに封入された微生物は、担体またはカプセルが崩壊 (分解) することによって環境中に外来微生物を拡散してしまうという懸念がある。加えて、拡散した微生物を回収することは困難である。さらに、担体に固定化またはカプセルに封入された微生物が一旦環境中に投入されると、ある程度生育した後、栄養分が不足して生育が止まり、浄化作用を発揮しなくなるという問題がある。このような場合は、外部から栄養分を与える作業が必要となる。また、環境中に投入された微生物はしばしば優秀な土着菌の存在により、その生育が阻害されてしまい、望むような浄化効果が得られないという問題がある。これら従来法の欠点は、弾力性に富んで耐久性があり、かつ物質の透過が可能であるシームレスカプセルに環境汚染物質分解微生物を封入することにより、解決可能と考えられた。
そこで、森下仁丹 (株) と長瀬産業 (株) は、前者の「バイオカプセル」技術と後者の微生物関連技術を組み合わせて、環境汚染物質分解微生物を内包するシームレスカプセル (図8) を共同開発した。環境汚染物質を透過する皮膜で構成されるカプセルの内部溶液に当該微生物を包み込み、カプセルをカラム、かご、袋等に封入することで水中に存在する対象汚染物質を分解除去する。微生物カプセルの利用によって、非常に簡易な装置で処理できると共に、分解プロセスがコンパクトになる、使用後のカプセルが回収できる等のメリットが考えられる。
環境汚染物質分解微生物を内包するシームレスカプセル (図9) は、物理的に強固で、幅広いpH領域でも長期間安定であり、ターゲット汚染物質が溶液からカプセル内部に効率的に透過するように皮膜構造 (網目サイズ、膜厚み) を調整することも可能である。ただし、環境汚染物質分解微生物が外部溶液に透過できないように、皮膜の網目サイズは細胞径 (0.5μm×1.0μm) 以下程度にする必要がある。
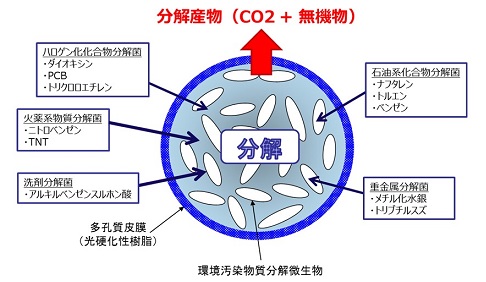
図9 環境浄化カプセルのコンセプト
6-4 シロアリ駆除剤カプセルの開発
シロアリは被害の甚大さと予防、駆除の困難さの点から見て、人類にとって最も厄介な害虫の一つである。シロアリは地中深く柱の中に巣を作り、その中心で卵を産むため、巣を完全に死滅させるには大量の液体殺虫剤を施工する必要がある。本行為は環境、人体への影響が問題となっており、少量の殺虫剤で速やかにシロアリの巣を駆除できる、シロアリ駆除剤の開発が求められている。
京都大学大学院の松浦らが発見した卵認識フェロモンを、殺虫剤を内包させたシームレスカプセルに塗布することで、シロアリが実卵と認識し、殺虫剤入りのカプセルを自ら巣の中枢まで運搬することを確認した。シロアリは乾燥防止や殺菌を目的に卵を舐めながら育てる習性があるため、シロアリの唾液中の成分で崩壊するカプセル皮膜を開発した。これにより、運搬中は殺虫剤が放出されず、巣の中で確実に殺虫剤が放出される画期的なカプセルを開発した。
本カプセルをシロアリの巣があると予測される周辺に餌と共に設置することで、黙っていてもシロアリの巣が駆除可能なシロアリ駆除システムとなる。コンセプトの模式図を (図10) に示す。尚、シロアリが卵と認識するには、カプセルのサイズと硬度を精密に制御する必要があり、目標値を外れると、たとえ卵認識フェロモンを塗布しても、ゴミとして認識されてしまうため、精度の高い製剤技術が必要となる。
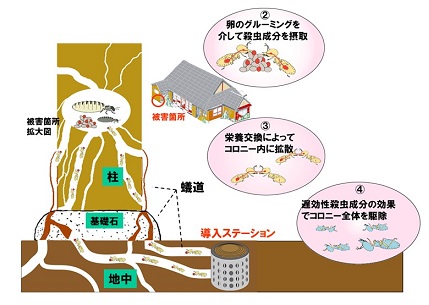
図10 カプセル型シロアリ駆除剤のコンセプト
7.最後に
物質を「包む」という一見シンプルな操作であるが、「包む」ことによって、これまで発現しえなかった様々な機能を発現することが可能となり、既存あるいは新規の物質同士の組み合わせによる可能性は、開発者のアイディアにより無限大に広がる可能性を秘めている。
本稿にて森下仁丹 (株) のシームレスカプセル技術、更にはカプセル全般の機能発現可能性他を理解頂き、開発者の新製品開発等のアイディアの一助となればと考える。
文献
1) 浅田雅宣: 第60回日本栄養改善学会学術総会要旨集 (2013).
2) 李雪駝、 他: 第16回日本食品微生物学会学術総会講演要旨集 (1995, 90).